원동신_편입기본_2강

역시 기초가 없다.
핏단기 ㅅㅌㅇ 강의 들을 때는 다 아는 것 같았는데
다 날아가 버렸다.
어디서 나 화학은 그래도 좀 하는데 라고 말하는 거 멈춰야겠다. 개쪽팔림
1. 분자구조의 기본은 비공유전자쌍 구하기
ClO₃- 에서 중심원자는 Cl
Cl- 비공유전자쌍 : [{Cl최외각전자7-(분자의 전하량-1)}-(산소갯수3개 * 산소이온화값2)] / 2 = {(7+1)-(3*2)} / 2 =1
결합차수S.N. = 산소갯수3 + 비공유전자쌍1 = 4
혼성오비탈 = (S.N=4) = sp³, 정사면체
루이스구조 그려보기

Cl-의 형식전하 = 최외각전자수7-다리갯수3-비공유전자수2=+2
Cl의 산화수 = 전체(-1) = O산화수(이온화값-2*갯수3) + Cl산화수
고로 Cl산화수 = -1 + 6 = +5
O의 형식전하 = 최외각전자수6-다리갯수1-비공유전자수6 = -1
*참고로 옥텟규칙을 확장해서 고려할 수도 있으니 편입에서는 특별한 언급이 없으면 위의 내용으로 분석함 (아래 사진은 그냥 참고만)

2. 같은 분자끼리의 결합은 대부분 무극성, 다른 분자끼리의 결합은 극성을 가짐 (왜? 전기음성도가 다르므로)
이온결합 = 금속원자 + 비금속원자
A원자와 B원자의 전기음성도 차이 > 0.3 : 극성
< 0.3 : 무극성
3. NH3 : sp3_비공유전자쌍1, 삼각뿔구조 : 107
NH4+ : sp3_비공유전자쌍0, 정4면체 : 109.5
NH2- : sp3_비공유전자쌍2, 굽은형 : 104 (비공유 전자쌍이 다리를 눌러 줘서 각이 줄어듦)
4.

5.
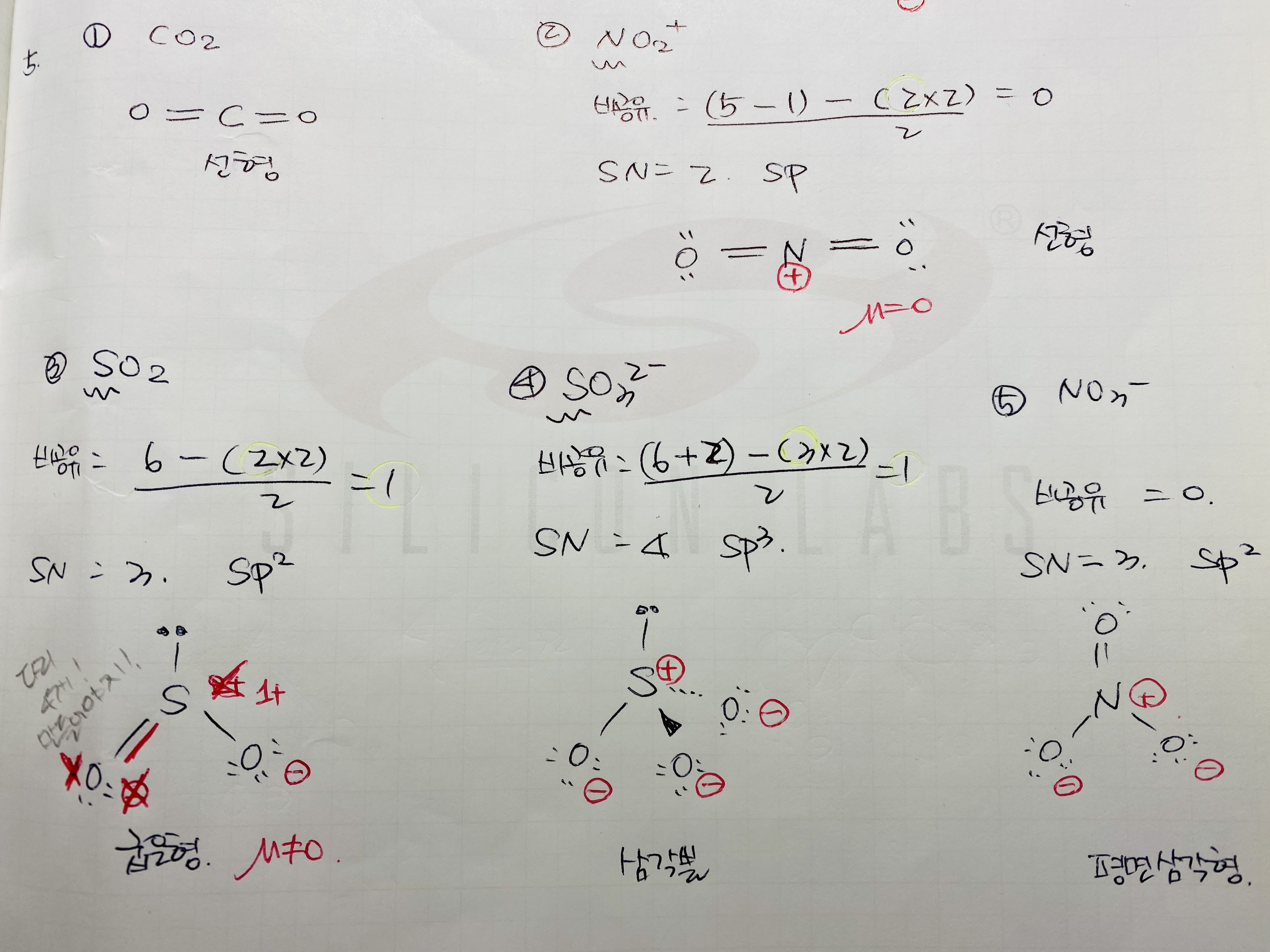
6. 결합각
NH3 : 삼각뿔, 107
CH4 : 정사면체, 109.5
NH4+ : 정사면체, 109.5
H₂O : 굽은형, 104.5
C₂H₂ : 일자형, 180
7. 쌍극자모멘트를 갖는다 = 극성을 갖는다 = 대칭이 아니라 치우친다
쌍극자모멘트를 갖지 않는다 = 무극성이다
NH3 : 삼각뿔, 극성 --> 쌍극자모멘트O
ClF3 : T형, 극성 --> 쌍극자모멘트O
XeF2 : 선형, 비극성 -->쌍극자모멘트X
CO2 : 선형, 비극성 --> 쌍극자모멘트X

8. 2번과 거의 유사한 문제
9. 전기음성도, F가 젤 큼, Fr이 젤 작음
같은 주기 : 오른쪽으로 갈 수록 커짐
극성크기 : 전기음성도 편차가 크면 클 수록 크다.
B-Cl > C-Cl
H-F > H-I
Cl-F < I-F
P-F > P-Cl
10. 결합길이가 짧은 것 --> 결합이 여러줄일 수록 더 짧다

11.

12.

13. OF2
{ 6-(2*1) }/2 = 2
SN = 4, sp3
14. SO3²-
{(6+2) - (3*2)} /2 = 1
SN = 4, sp3
CO3²-
{(4+2) - (3*2)} / 2 =0
SN = 3, sp2
15. SO3 : #4참조
PCl4+ : #11 참조
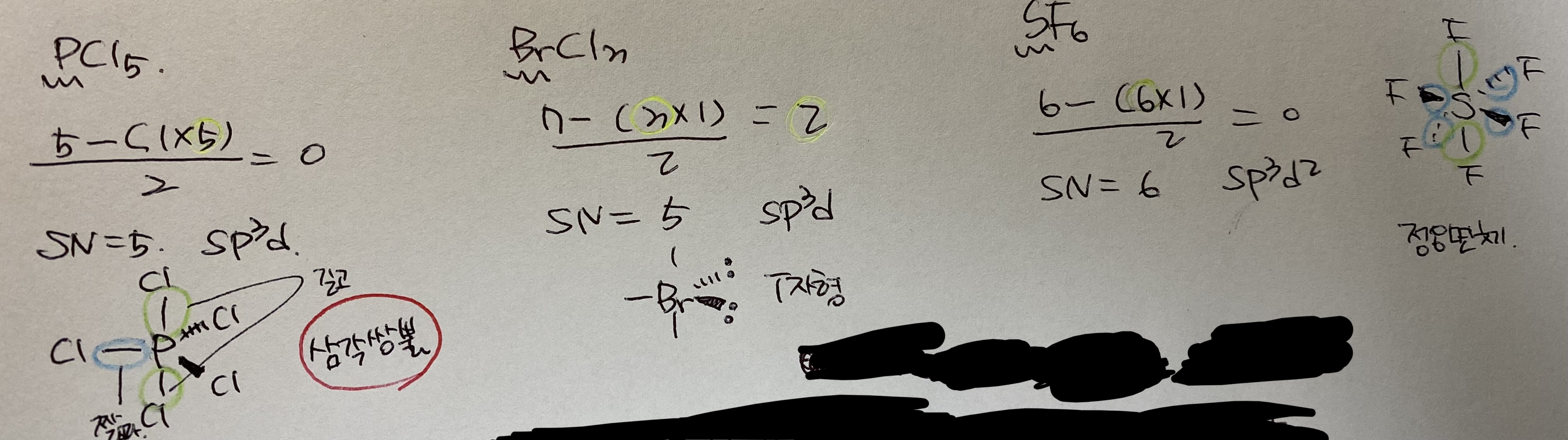
16. 중심원자의 혼성 = 혼성오비탈
NH₃ : (5-3*1)/2 = 1, SN=4, sp3
NH4+ : {(5-1) - (4*1) }/2 = 0, SN=4, sp3
NO₂+ : {(5-1) - (2*2) }/ 2 = 0, SN=2, sp
NO₂- : {(5+1) - (2*2) } / 2 =1, SN=3, sp2
PF₃ : {5-(3*1)} /2 = 1, SN=4, sp3
PF5 : {(5-(5*1)} / 2 = 0, SN=5, sp3d
BF₃ : {3-(3*1)} / 2 = 0, SN=3, sp2
BF4- : {(3+1) - (4*1)} / 2 = 0, SN=4, sp3
17. BrF5 : {7 - (5*1)} / 2 = 1, SN=6, sp3d2
BrF3 : {7-(3*1)}/2 = 2, SN=5, sp3d
AsCl5 : {5-(5*1)} / 2 = 0, SN=5, sp3d
CF₃+ : {(4-1) - (3*1)} / 2 =0, SN=3, sp2
BeF₃- : {(2+1)-(3*1)}/2 = 0, SN=3, sp2
18.

19.

20. H₂O : 굽은형
OF₂ : 굽은형
CO₂ : 선형
BeH₂ : 선형
SiO₂ : 선형
21. SO₂ : 굽은형, H₂O : 굽은형
NH₃ : 삼각뿔, H₃O+ : 삼각뿔
CH₄ : 정사면체, NH₄+ : 정사면체
CO₂ : 선형, NO₂- : 굽은형
22. SF4 : {6-(4*1)}/2 = 1
SN = 5, sp3d

비공유 전자쌍 : 3*4 + 1 = 13